Fda 医療 機器
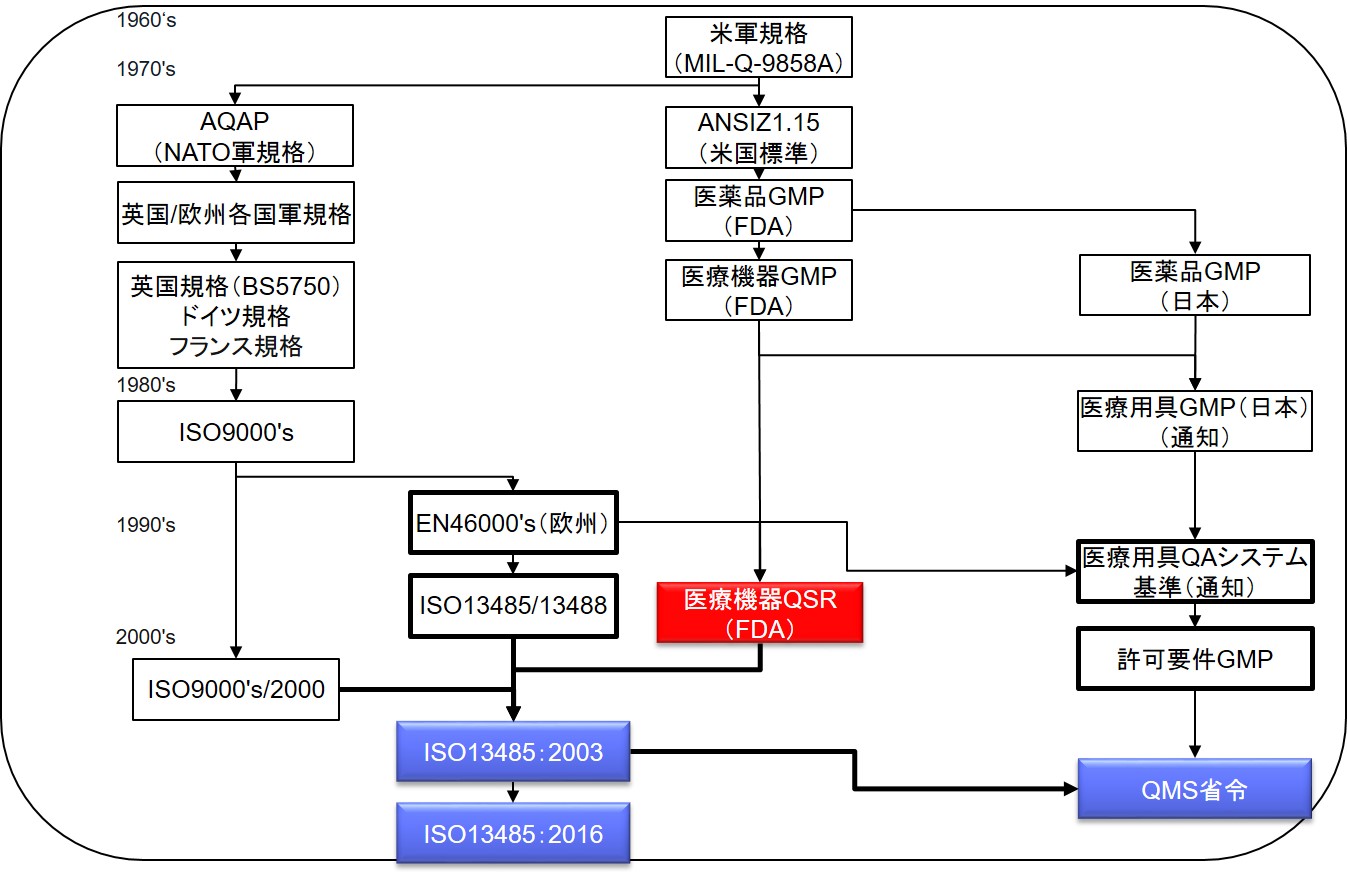
医療機器に関する品質規則

リアルワールドエビデンスに基づく医療機器開発の時代へ 海外医療技術トレンド 28 1 3 ページ Monoist
米国在住医療機器コンサルタントによる米国進出セミナー Fda規制対応 戦略立案 アメリカ医療の最新情報 Fda最新情報 提携セミナー アイアール技術者教育研究所 製造業エンジニア 研究開発者のための研修 教育ソリューション

医療機器の知識 Fdaの承認審査プロセス 石居昭夫 本 通販 Amazon

Fda Udi 規格適合 Nicelabel
Fda 510 K 申請 グロービッツ
医療機器修正法(MDAA) 1976 医療機器安全法(SMDA) 1990 FDA近代化法(FDAMA) 1997 医療機器ユーザーフイー及び近代化法 (MDUFMA)02 6 連邦食品、医薬品及び化粧品法(FD&CA) • 法律の英文標題Federal Food, Drug, and Cosmetic Act • 医療機器規制の基本法である。.

Fda 医療 機器. 1/3付で米国FDAから「CDRH to Post Early Notification of Recalls」と題した通知として、「What is a Medical Device Recall?」ウェブサイトを公開しています。 本ウェブサイトには、“Recall”の定義と共に、 情報データベースとリンクさせています。 米国FDAとしての“recall”とは、医療機器の不具合・ 患者への健康. 医療機器のアジア法規制対応はクアルテックジャパンコンサルティング nmpa, tfda, hsa, mda, mdd, pfda, moh, thai fda, ce mark 〒 大阪府大阪市西区京町堀3丁目921 理工ビル. 米国における医療機器開発にかかる行政は, 米国医薬食品局(Food and Drug Administration;.
国FDAのUDIデータベースにほぼ準拠した ものとなっている. ( )30 医機学 Vol.85,No.3(15) ― ― 表1 FDA医療機器UDI規制 施行スケジュール 346 p 特集_黒澤氏indd 30. 1/3付で米国FDAから「CDRH to Post Early Notification of Recalls」と題した通知として、「What is a Medical Device Recall?」ウェブサイトを公開しています。 本ウェブサイトには、“Recall”の定義と共に、 情報データベースとリンクさせています。 米国FDAとしての“recall”とは、医療機器の不具合・ 患者への健康. 高リスク機器の場合のfdaの審査等 ・審査期間:30日 ・申請に対するfdaの対応:承認、条件付き承認、非承認 fdaの立入検査、問題のある場合の措置等: ・医療機器を用いた臨床研究について、fdaはgcp査察等を実施。.
Joseph Tartal(USFDA) ,“Corrective and Preventive Action Basics,” Nov 4th, 14 Slide 9 ⼿順の前提 (是正・予防措置を実施するための)⼿順 は、配送済の医療機器については、取るべ き管理と措置を提供し、まだ未配送のもの は、不適合となる潜在的可能性をもってい. 医療機器は GHTF (医療機器規制国際整合化会議:Global Harmonization Task Force) のルールを参考として、各国でクラス分類されています。 日本の医療機器は、「 薬機法* 」によりクラスⅠ~Ⅳに分類され、厚生労働省により告示されています。. 医療機器修正法(MDAA) 1976 医療機器安全法(SMDA) 1990 FDA近代化法(FDAMA) 1997 医療機器ユーザーフイー及び近代化法 (MDUFMA)02 6 連邦食品、医薬品及び化粧品法(FD&CA) • 法律の英文標題Federal Food, Drug, and Cosmetic Act • 医療機器規制の基本法である。.
米国食品医薬品局(FDA)は、米国民の健康を守るため、米国に医療機器を輸出する海外の製造業者に対して定期的に査察を実施しています。 これは、日本の薬事法のGMP監査に相当するもので、FDAのGMPはQSR( Quality System Regulation )品質システム規制に基づく査察が行われます。. 1/3付で米国FDAから「CDRH to Post Early Notification of Recalls」と題した通知として、「What is a Medical Device Recall?」ウェブサイトを公開しています。 本ウェブサイトには、“Recall”の定義と共に、 情報データベースとリンクさせています。 米国FDAとしての“recall”とは、医療機器の不具合・ 患者への健康. FDAユニークデバイス識別システム規則とは 以下、米国FDAの医療機器に対するユニークデバイス識別システム規則を解説する。 ⅠUDIシステムの構築手順 ユニークデバイス識別(Unique Device Identification)システム規則は略称して「UDIシステム規 則」と呼ばれる。.
米国に医療機器を輸出しようとする場合、米国食品医薬品局(FDA:Food and Drug Administration)への届出・承認申請が必要です。 FDAで医療機器の規制を管轄する部署は、医療機器・放射線保健センター(CDRH:Center for Devices and Radiological Health)です。. 米国食品医薬品局(FDA)は、米国民の健康を守るため、米国に医療機器を輸出する海外の製造業者に対して定期的に査察を実施しています。 これは、日本の薬事法のGMP監査に相当するもので、FDAのGMPはQSR( Quality System Regulation )品質システム規制に基づく査察が行われます。. FDAは「連邦食品医薬品化粧品法」(Federal Food, Drug, and Cosmetic Act FDCA)および特別法「医療機器修正法」(Medical Device Amendment Act, 1976年制定)など[注]に基づいて、約1,700種ある医療機器を歯科、心臓・循環器科、放射線科、免疫学関係等、17の医療専門分野 (medical specialty panels)に分類し、さらに患者や機器使用者に影響を及ぼす可能性のあるリスクの程度によって3クラス(Class I、IIおよびIII)に分けています。.
FDAは「連邦食品医薬品化粧品法」(Federal Food, Drug, and Cosmetic Act FDCA)および特別法「医療機器修正法」(Medical Device Amendment Act, 1976年制定)など注に基づいて、約1,700種ある医療機器を歯科、心臓・循環器科、放射線科、免疫学関係等、17の医療専門分野. FDA)において医療機器行政を所管する Center for Devices and Radiological Health (CDRH)において,Investigational Device Exemptio(nIDE)制度を軸として実施されている..

Mit Tech Review 米fda Ai医療機器の新たな規制枠組みを検討

最新ニュース クアルテックジャパンコンサルティング株式会社

個人用心電図デバイス開発のalivecorが医療機器ソフトでもfda認定を取得 Techcrunch Japan

米国規制最新動向 メドテックステーション Medtech Station Com
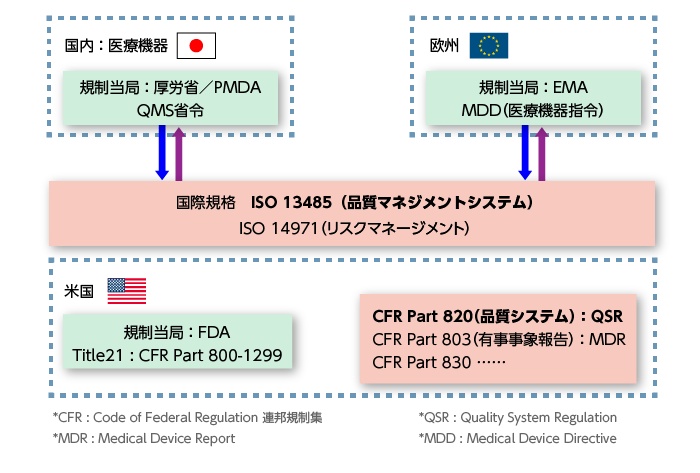
Plmソリューション Enovia 医薬品 医療機器業界向け 東芝デジタルソリューションズ

越境ec 米国向け販売で守るべき Fdaルール とは Live Commerce ブログ
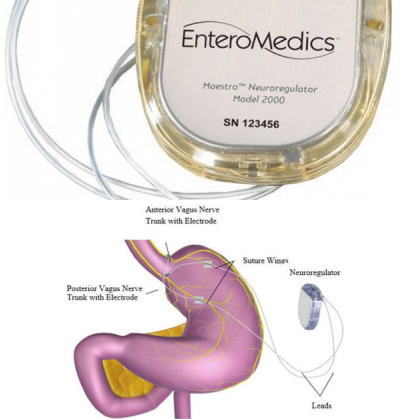
Fdaは体内埋め込み型の減量の医療機器を承認 くすりなひと

米国kaatsu Global社製kaatsu専用デバイス Kaatsu Nano が医療機器として米国fdaに承認されました Kaatsu Japan株式会社のプレスリリース
医療機器認証のカテゴリー変更 ジェトロなどが解説のセミナー開催 タイ ビジネス短信 ジェトロ

医療機器メーカーは 品質管理プロセスを制御することで革新的な製品をいち早く市場に投入できる Ptc

医療機器ソフトウェア規制の最新状況 1 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

オンデマンドセミナー Fdaが医療機器のヒューマンファクタエンジニアリングに期待すること

Fda 510 K 申請 グロービッツ
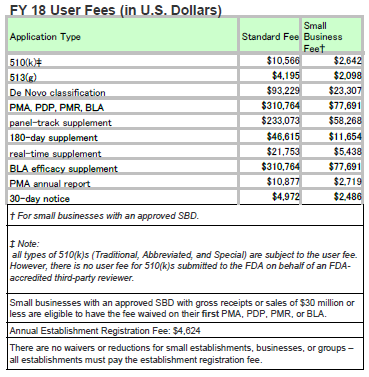
米国fda 18年度料金 10月1日 無線 医療機器の規格
Http Www Dsri Jp Gshealth Disclosure Pdf Fda Udi Pdf
Fda医療機器 De Novo グロービッツ

医療機器の変更管理 医薬 製薬 医療機器企業向けピンポイントニュース ブログ

痩身用語 Fdaアメリカ医療機器承認って何

日米欧の医療機器規制の概略比較です 無線 医療機器の規格
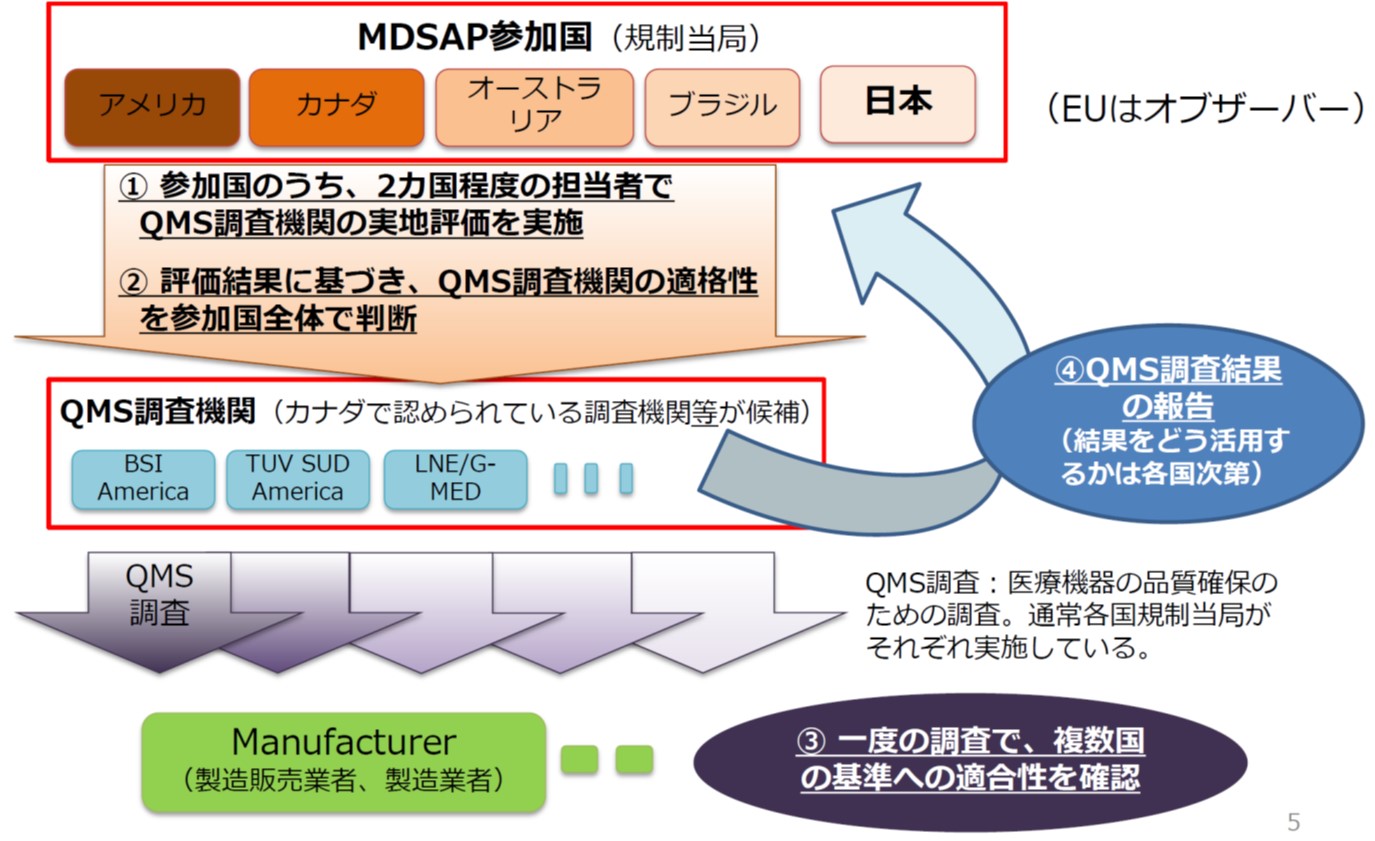
Mdsapとは イーコンプライアンス
Arc Asahi Kasei Co Jp Report Arc Report Pdf Rs 1044 Pdf
Www Med Device Jp Pdf State Summary Amed15 Marketing 1b Regulation Pdf

日本でapple Watch 米国でgalaxy Watchの心電図アプリ使えず Iphone Mania

医療機器fda Mdsapコンサルタント 医療機器コンプライアンスサポート合同会社

Fda 医療機器の認定規格リストを更新 無線 医療機器の規格
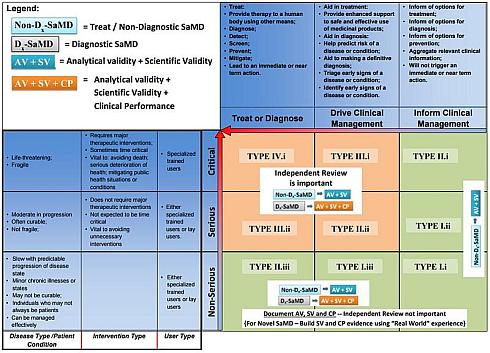
海外で進む医療ソフトウェア臨床評価の標準化 海外医療技術トレンド 1 2 ページ Monoist
Www Med Device Jp Pdf State Summary Amed15 Marketing 1b Regulation Pdf

Fdaによる法的措置 イーコンプライアンス

米国における医療機器規制プロセス ー重要課題の考察 検討 解説ー 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

医療機器におけるユーザビリティとfdaガイダンス Manualzz
Www Med Device Jp Pdf State Summary Amed15 Marketing 1b Regulation Pdf
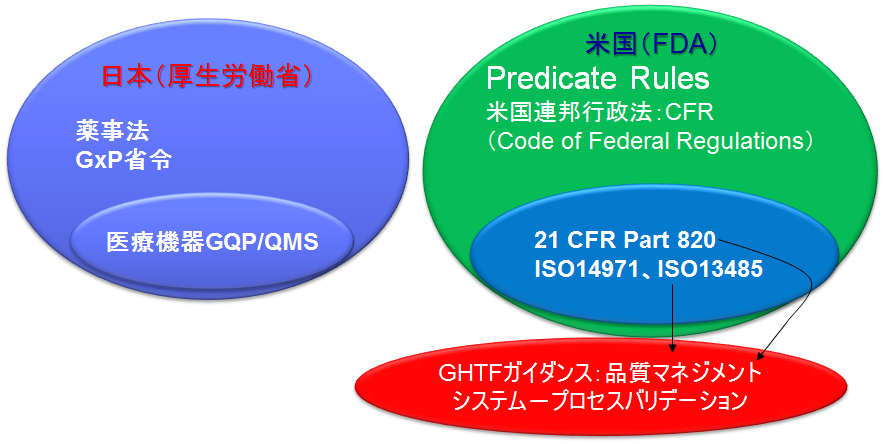
医療機器に関する品質規則

楽天市場 イオンスパ Bath1000a プレミアムシャワーヘッド 米国fda医療機器 登録 Iso Iso9001取得 Jmp 総合卸ヨシムラ

Whillの車いすが米国fda認可を取得 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

Fdaの医療機器相談業務 Pre Submission 申請前プログラム 通称q Sub 株式会社 日本医療機器開発機構 Jomdd

米国はバイデン政権へ移行 医療機器のイノベーション支援策はどうなるのか 1 3 Monoist
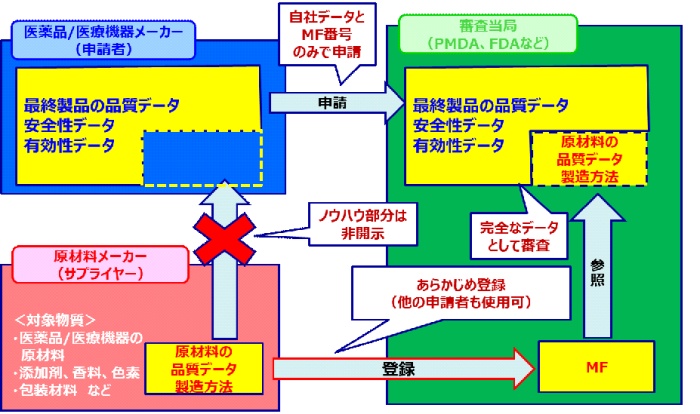
医療機器材料の海外マスターファイル Mf 登録支援サービス 海外mf Dmf 作成サービス 医療機器 医療材料 サービス 株式会社住化分析センター

保存版 医療機器の開発プロセス 事業計画とその全体像 第2弾 薬事規制の重要性 株式会社 日本医療機器開発機構 Jomdd

Fda医療機器 製品クラス分類調査 グロービッツ

医療機器 業種別で探す 品質マネジメントシステム Qms ならマスターコントロール

Fdaがバイオマーカ型医療機器開発ツール Mddt を初認証
Fda医療機器 市販前認可 グロービッツ
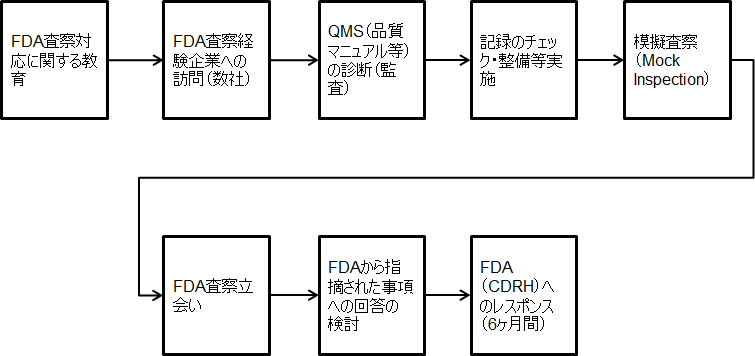
医療機器企業向けコンサルテーション Fda査察対応支援 イーコンプライアンス
Http Www Dsri Jp Gshealth Disclosure Pdf Fda Udi Pdf

Fda Ceマーク を徹底比較 中国マスクバブル崩壊から見る Fda Ceマーク認証 のメリット アメリカ 海外進出ノウハウ Digima 出島
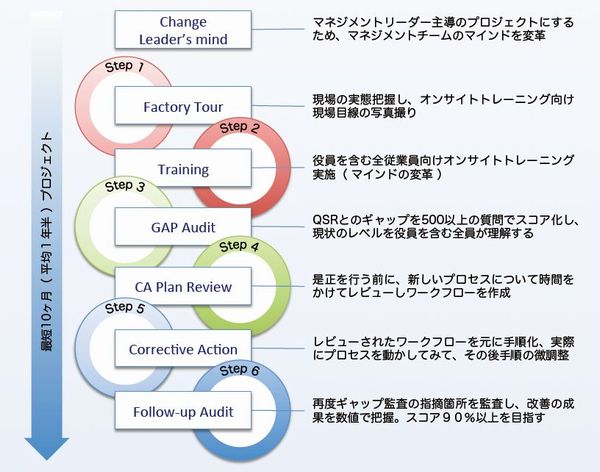
査察対応プロジェクトについて 医療機器 Fda クオリス イノーバは Fda のエキスパートです
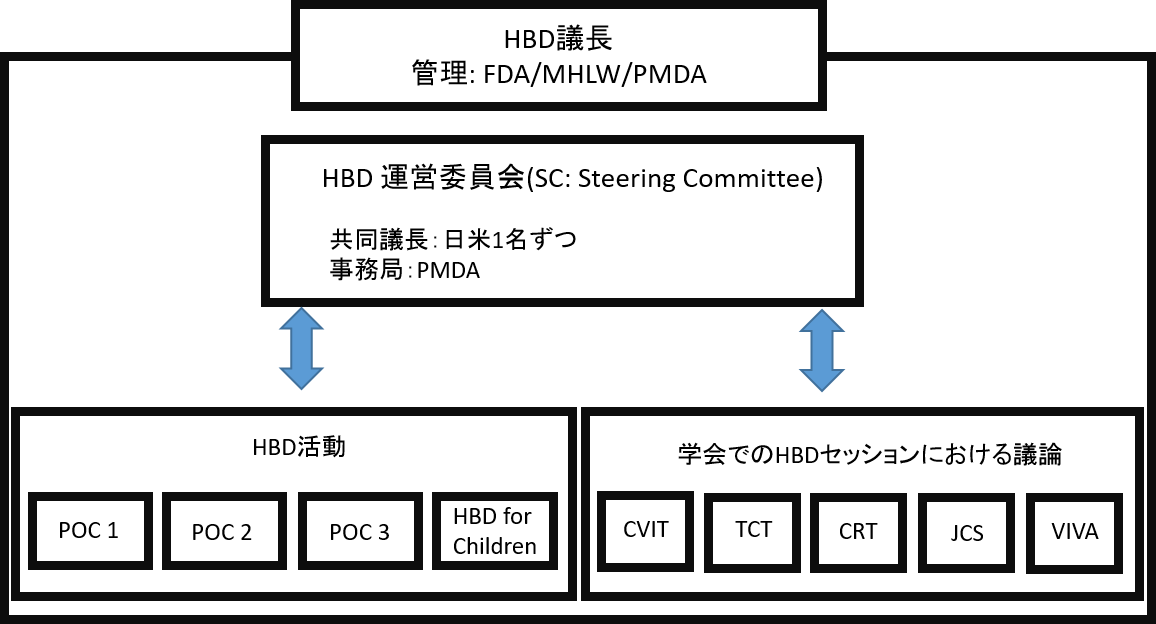
Hbd Harmonization By Doing 独立行政法人 医薬品医療機器総合機構

医者に代わり診断を下すai医療機器 Idx Dr が米国で初めて認可 糖尿病網膜症を1分で判定 Roboteer ロボティア

医療機器企業におけるソフトウェアバリデーション

政策研ニュース 日米のsoftware As A Medical Deviceの新たな規制枠組み構築動向
Http Www Jfmda Gr Jp Metis Guidebook Pdf 1801 1801 01 Pdf
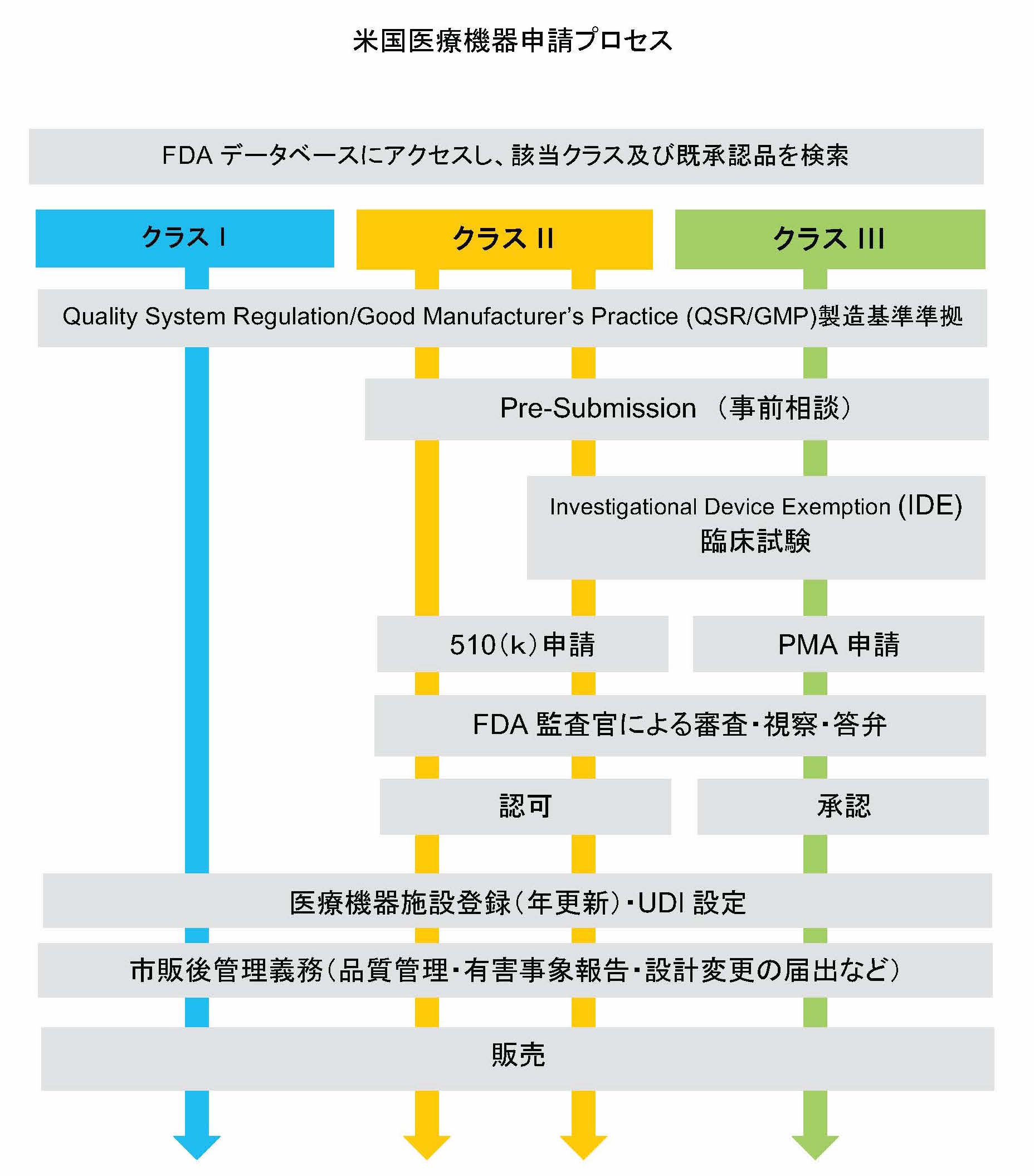
医療機器の輸出 アメリカfdaの手続をざっくりとまとめてみました 株式会社ac Medi
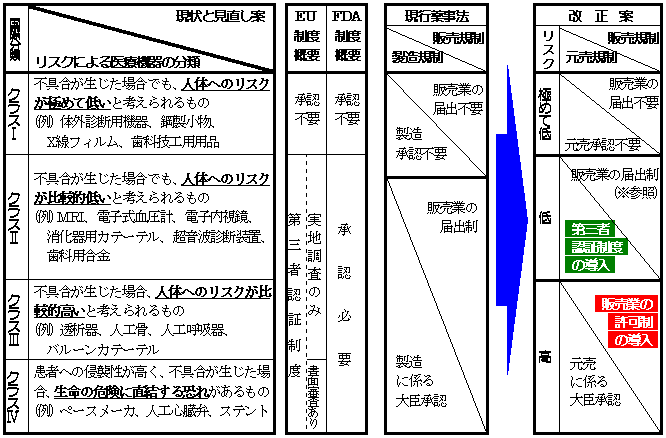
医療機器に係る カテゴリー と 安全対策 の見直し

楽天市場 イオンスパ Bath1000a プレミアムシャワーヘッド 米国fda医療機器 登録 Iso Iso9001取得 Jmp 総合卸ヨシムラ

Fda医療機器登録メーカー サプライヤー 卸売業者 流通業者 および工場からのfda医療機器登録について知っておくべきこと

医薬品 医療機器業界向けictソリューション トップ 東芝デジタルソリューションズ

Fda医療機器 510 K

米国fdaが強化を求める医療機器のサイバーセキュリティ 海外医療技術トレンド 10 1 3 ページ Monoist

Fda 最新情報 医療機器申請の新しい変更について 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

医療機器のul およびfda 規格への適合を支援する方法 ソフトウェア インテグリティ

Fda医療機器申請戦略の構築 グロービッツ

Fdaユーザビリティ試験の動向 510 K 申請の洞察 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

医療機器の知識 Fdaの承認審査プロセス 石居昭夫 本 通販 Amazon

米国fda レーザー機器規則の概要 Ceマーク Emc 製品安全emc 製品安全規格 Ceマーキングの情報

Hal 下肢タイプ タイ Fda の医療機器承認を取得 ロボケアセンター 脳梗塞 脳出血 脊髄損傷の後遺症 介護リハビリを支援

Fda査察対応支援サービスで 日本の医療機器メーカーの海外市場展開を支援する 3ページ目 日経クロステック Xtech

全3講 製薬企業 医療機器企業におけるfdaが要求するcapa導入の留意点 第1講 Youtube

楽天市場 イオンスパ Bath1000a プレミアムシャワーヘッド 米国fda医療機器 登録 Iso Iso9001取得 Jmp 総合卸ヨシムラ

Fdaがニチノール含有医療機器の市販前審査提出物等のドラフト版

医療機器ソフトウェア規制の最新状況 1 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

Cufitec高性能マスク がfdaの医療機器認証取得 Nbcメッシュテック 食品産業新聞社ニュースweb

第回医療機器等事業化促進プラットフォームセミナー 米国医療機器市場とiso 医療機器への参入とqmsの構築 公益財団法人神戸医療 産業都市推進機構
米fda 医療機器へのサイバー攻撃の可能性を警告 写真1枚 国際ニュース Afpbb News

保存版 医療機器の開発プロセス 事業計画とその全体像 第2弾 薬事規制の重要性 株式会社 日本医療機器開発機構 Jomdd

Fdaが21年度の新しい医療機器とジェネリック医薬品のユーザー料金を発表 Registrar

Fdaの基礎知識 Fda認証が必要な商品 取得方法 罰則とは アメリカ 海外進出ノウハウ Digima 出島

Fdaによるpma承認率が近年では最高に 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト

米国fdaが市販前医療機器サイバーセキュリティ管理指針改訂草案を公表 サービス サイバーリスク デロイト トーマツ グループ Deloitte

医療用hal 米国fda 理学療法士 作業療法士 言語聴覚士の求人 セミナー情報なら Post

米国fda 医療機器規制はどのような内容か No 1 無線 医療機器の規格
Www Med Device Jp Pdf State Summary Amed15 Marketing 1b Regulation Pdf

医療機器の輸出 アメリカfdaの手続をざっくりとまとめてみました 株式会社ac Medi
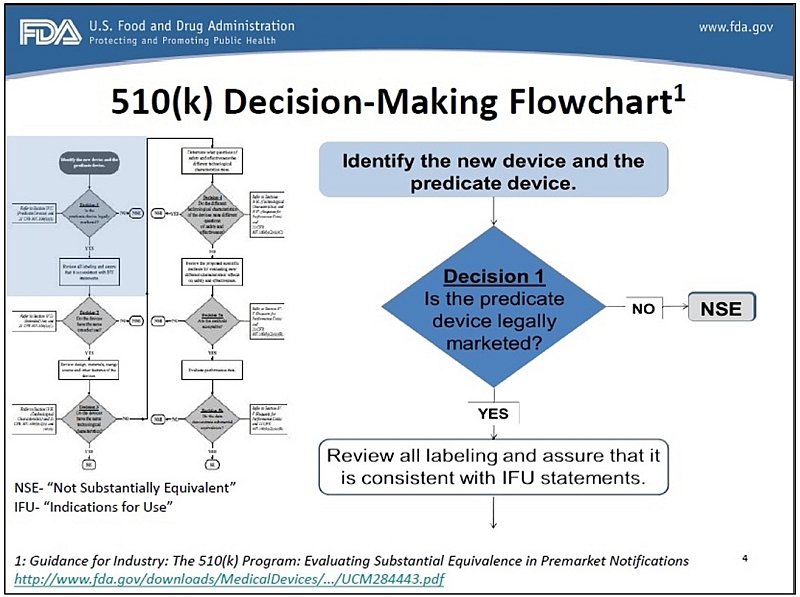
米国が強化を進める手術ロボットの安全対策 海外医療技術トレンド 5 1 3 ページ Monoist

Fdaの医療機器相談業務 Pre Submission 申請前プログラム 通称q Sub 株式会社 日本医療機器開発機構 Jomdd

医療機器のための米国fda Udi規則 Youtube

無線 医療機器の規格 医療機器
医療機器メーカー向けサービス

医療機器の製造製品品質の卓越化 Siemens Digital Industries Software

Yc出身 企業のfda承認を支援するクラウドサービスの Enzyme Healthtechnews

医薬品 医療機器fda対応マニュアル 本 通販 Amazon

医療機器の輸出に向けた海外の認証取得の費用を補助します 令和元年度海外認証等取得補助金の公募を開始 埼玉県
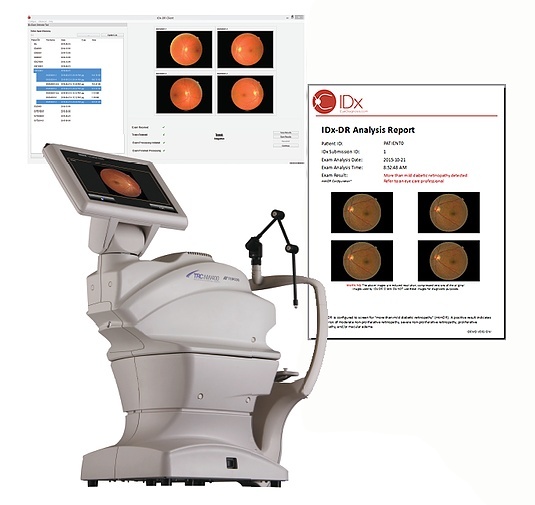
Aiが医師なしで糖尿病による網膜症を診断 Fdaが検査装置 Idx Dr を認可 Cnet Japan

米国fda 医療機器規制はどのような内容か No 2 無線 医療機器の規格

ますます厳格化するfda査察を教育訓練ictで支援 1 医療機器の製造 開発 展示会 セミナー Medtec Japan 東京ビッグサイト



